Pharma GMP Compliance
Data Integrity Kit
52% aller FDA-Findings betreffen Data Integrity
Data Integrity Mängel dominieren FDA Warning Letters und 483 Observations seit Jahren.
Generic Logins, deaktivierte Audit Trails, unvalidierte Excel-Sheets – Inspektoren kennen die Schwachstellen.
Das Problem: Die meisten Pharma-KMUs wissen, dass sie DI-Lücken haben. Was fehlt: ein strukturierter Ansatz zur Gap-Analyse und Remediation – ohne teure Berater.
Die Lösung: Ein komplettes Toolkit zur Selbstbewertung und Behebung. Gap Assessment, Risk Matrix, SOPs, und 44 echte Inspektionsfragen – alles was Sie brauchen, um vor der nächsten Inspektion compliant zu sein.
Scrollen Sie durch die 8 Dokumente. Links sehen Sie Vorschauen, rechts die Erklärung zur Anwendung. Am Ende können Sie das Bundle kaufen und sofort einsetzen.
Komplettes Data Integrity Kit – sofort einsatzbereit.
Jetzt kaufen →Sichere Zahlung via Gumroad · Sofort-Download
Enthalten:
- ✓8 Dokumente (Word, Excel, PDF)
- ✓Gap Assessment mit 93+ Formeln
- ✓Ausgefülltes Beispiel (PharmaPro GmbH)
- ✓44 Inspector Questions
- ✓12 Red Flags Checklist
- ✓Firmenweite Lizenz
Lücken finden – Gap Assessment Tool
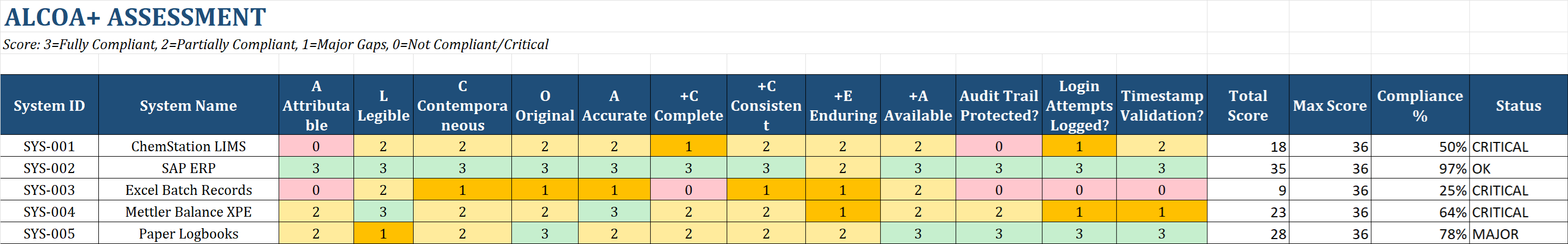
Warum zuerst das Assessment?
Sie können nur fixen, was Sie kennen. Das Gap Assessment Tool ist Ihre zentrale Datenbank für alle GxP-relevanten Systeme.
Was das Tool erfasst:
- • System Inventory: Alle GxP-Systeme mit GAMP-Kategorie
- • ALCOA+ Bewertung: Alle 9 Attribute (nicht nur 5!)
- • Generic Logins: Eigene Spalte – der #1 FDA-Finding
- • Audit Trail Status: Enabled/Disabled/N.A.
- • Compliance Score: Automatisch berechnet (93 Formeln)
💡 Das Dashboard zeigt sofort die kritischsten Lücken – perfekt für Management Review.
Anforderungen definieren – Data Integrity Policy
Die Basis für alles Weitere
Ohne Policy keine Compliance. Diese SOP definiert Ihre ALCOA+ Anforderungen, Rollen und Verantwortlichkeiten.
Enthaltene Kapitel:
- • ALCOA+ Definitionen: Alle 9 Attribute erklärt
- • Rollen: DI Officer, System Owner, Process Owner
- • Audit Trail Requirements: Wann, wie, wer?
- • Access Control: Keine Generic Logins!
- • Periodic Review: Risikobasierte Frequenz
- • Escalation: Critical → Major → Minor
📋 Review-Frequenz ist risikobasiert per ICH Q10 – nicht starr alle 2 Jahre.
Risiken bewerten – GAMP 5 Risk Matrix
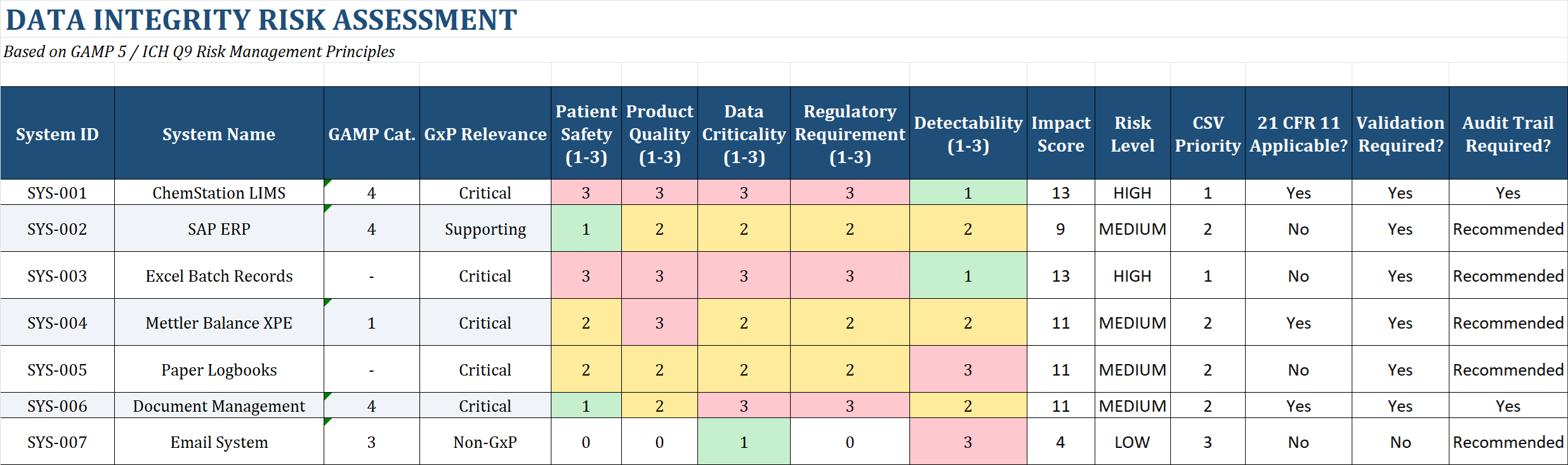
Nicht alles validieren – das Richtige validieren
Die Matrix hilft Ihnen, Validierungsaufwand risikobasiert zu priorisieren – genau wie GAMP 5 es fordert.
Features:
- • GAMP 5 Kategorien: 1, 3, 4, 5 + Spreadsheet
- • Risk Scoring: Impact × Detectability
- • 21 CFR 11 Scope: Automatisch berechnet
- • Risk Acceptance: HIGH/MEDIUM/LOW Kriterien
- • Validation Priority: Direkte Handlungsempfehlung
✓ Die Risk Acceptance Criteria sind neu in v1.1 – ein häufiges Audit-Finding.
Audit Trails prüfen – Review SOP
Der unterschätzte Prozess
Die meisten haben Audit Trails aktiviert – aber niemand schaut sie an. Diese SOP macht Audit Trail Review zum Routineprozess.
Enthaltene Sektionen:
- • Review-Typen: Batch Release, Periodic, For-Cause
- • 12 Red Flags: Was Inspektoren suchen
- • Eskalationspfad: 4h / 24h / 5 Tage
- • Appendix: Fertiges Review-Formular
12 Red Flags – Was Inspektoren suchen:
- ⚠️ Änderungen außerhalb der Arbeitszeit
- ⚠️ Änderungen kurz vor Batch Release
- ⚠️ Fehlende Reason for Change
- ⚠️ Test-Wiederholungen ohne OOS
- ⚠️ Gelöschte Daten
- ⚠️ Sequenz-Lücken
⚠️ Neu in v1.1: Expliziter Verweis auf Batch Release SOP – ein früheres Review-Finding.
Maßnahmen planen – Remediation Plan Template
Strukturiert zur Compliance
Gap gefunden – und jetzt? Der Remediation Plan gibt Ihnen eine 4-Phasen-Struktur mit realistischen Zeitvorgaben.
Die 4 Phasen:
- • Phase 1 (0-4 Wochen): Quick Wins – Audit Trail aktivieren, Generic Logins eliminieren
- • Phase 2 (1-3 Monate): Prozesse – SOPs, Access Review, Periodic Review
- • Phase 3 (3-6 Monate): Systeme – CSV, LIMS-Upgrade, E-Signatures
- • Phase 4 (6-12 Monate): Kultur – KPIs, Management Review, Annual Assessment
💼 Enthält Budget-Felder – wichtig für Management Buy-In.
Auf die Inspektion vorbereiten – 44 Inspector Questions
Wissen, was kommt
Diese 44 Fragen sind keine Theorie – sie basieren auf echten FDA-, EMA- und PIC/S-Inspektionen 2020-2024.
Kategorien:
- • Governance (10): Policy, Training, DI Officer
- • Electronic Systems (12): Audit Trails, Generic Logins, Access
- • Specific Systems (8): Excel, Standalone, LIMS
- • Data Handling (6): OOS, Complete Data, Re-Analysis
- • Backup (4): Backup, Restoration Test, Retention
- • Paper (4): GDP, Corrections, Blank Forms
Beispiel-Fragen:
- "Can the audit trail be disabled? By whom?"
- "Show me a list of all GxP computerized systems."
- "Do you use any generic or shared login accounts?"
🎯 Üben Sie die Antworten mit Ihrem Team – vor dem Audit, nicht währenddessen.
Für den Schreibtisch – Quick Reference Card
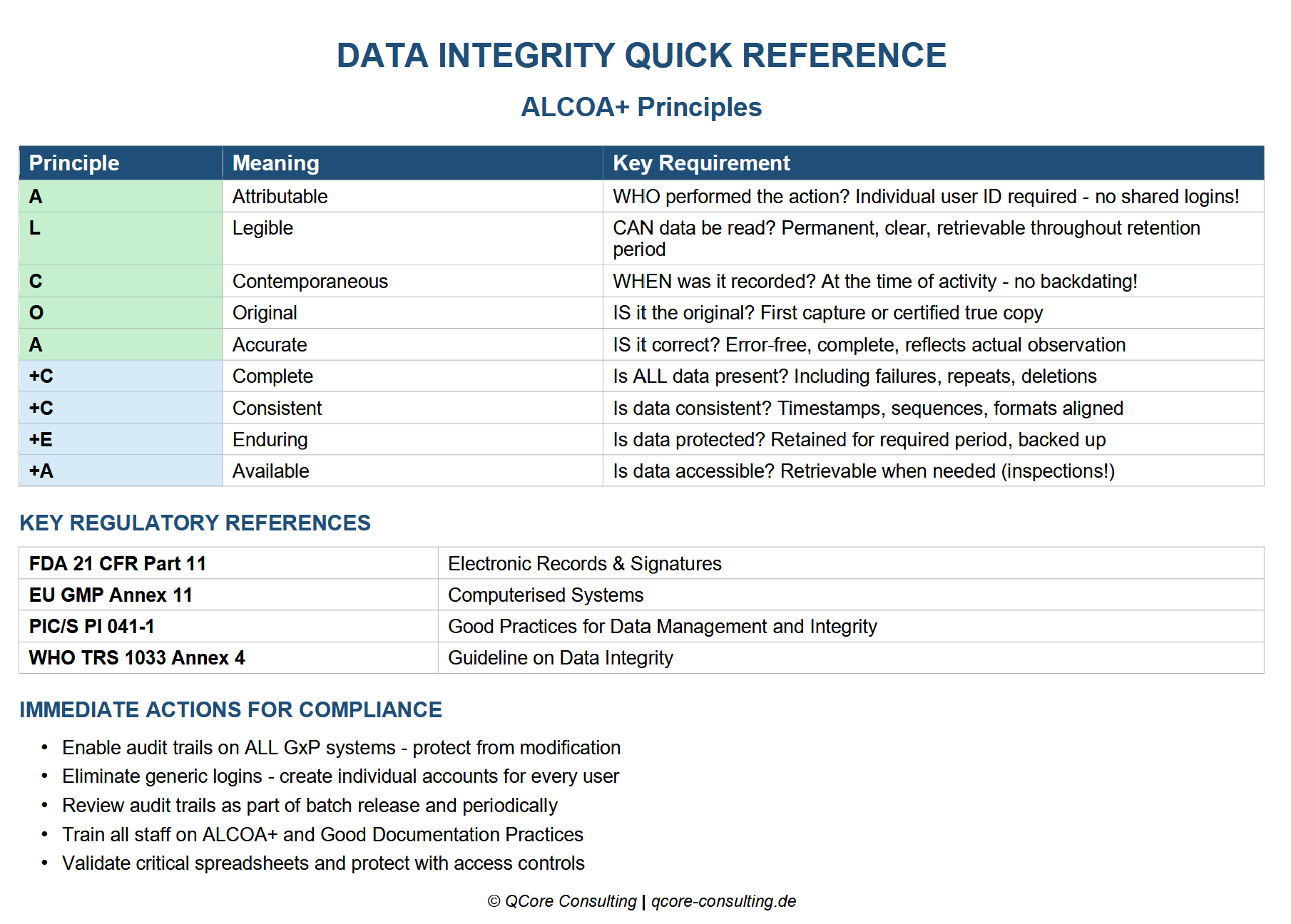
ALCOA+ auf einen Blick
Ausdrucken, laminieren, aufhängen. Die Quick Reference fasst ALCOA+ und die 12 Red Flags visuell zusammen.
Inhalt:
- • ALCOA+ Prinzipien erklärt
- • 12 Red Flags Checklist
- • Escalation Path (Critical/Major/Minor)
- • Golden Rules of Data Integrity
🖨️ Ideal fürs Labor oder QC-Büro – erhöht die Awareness am Shopfloor.
So sieht's fertig aus – PharmaPro GmbH Example
Lernen am echten Beispiel
Keine geschönten Zahlen – dieses Beispiel zeigt ein realistisches Assessment mit 62% Compliance Score und echten Findings.
Das Szenario:
- • Unternehmen: PharmaPro GmbH, Munich (45 MA)
- • Systeme: 7 GxP-Systeme bewertet
- • Score: 62% – CRITICAL
- • Hauptprobleme: LIMS Audit Trail aus, Generic Login "Lab", Excel unvalidiert
- • Budget: €15.700 Remediation-Kosten geschätzt
Kritische Findings im Beispiel:
- ✗ ChemStation LIMS: Audit Trail DISABLED
- ✗ Generic Login "Lab" von 8 Analysten genutzt
- ✗ Excel Batch Records: Keine Access Controls
✓ Nutzen Sie das Beispiel als Trainingsreferenz – zeigt, dass es okay ist, Lücken zu finden.
Data Integrity ist nur der Anfang
Ein vollständiges Pharma QMS braucht mehr. Kombinieren Sie das DI-Kit mit unseren anderen Bundles.